Un medicamento de Roche, uno de los principales productos contra el cáncer de la compañía, se está expandiendo a las enfermedades autoinmunes con un nuevo fármaco Aprobación de la FDA para la nefritis lúpica.
El fármaco Gazyva, de infusión intravenosa, ahora se puede utilizar para tratar a adultos con nefritis lúpica activa que reciben el tratamiento estándar para la enfermedad. La decisión regulatoria anunciada el lunes trae otra terapia biológica para la enfermedad junto con un producto de gran éxito de GSK.
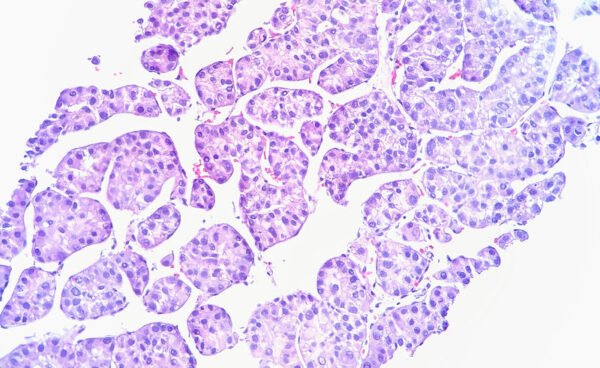
La nefritis lúpica ocurre como una complicación del lupus eritematoso sistémico, una enfermedad en la que el sistema inmunológico ataca por error los propios tejidos y órganos del cuerpo. En la nefritis lúpica, los autoanticuerpos causan inflamación de los riñones, lo que provoca la pérdida de nefronas, las unidades funcionales de los riñones que filtran la sangre para producir orina. La pérdida irreversible de nefronas conduce al deterioro de la función renal; Muchos pacientes desarrollan una enfermedad renal terminal que requiere diálisis o un trasplante de riñón. Según Roche, más de 1,7 millones de personas en todo el mundo padecen nefritis lúpica, la mayoría de ellas mujeres.
Gazyva actúa descomponiendo las células B, un tipo de célula inmunitaria. El fármaco es un anticuerpo monoclonal diseñado para unirse a CD20, una proteína que se encuentra en la superficie de las células B. Este enfoque desencadena mecanismos que conducen a la muerte celular. Las células B anormales pueden causar cáncer de sangre y Gazyva se aprobó por primera vez en 2013 para tratar la leucemia linfocítica crónica. Pero las células B también pueden provocar inflamación persistente en enfermedades autoinmunes, y Gazyva es el último ejemplo de un fármaco contra el cáncer que encuentra nuevos usos en inmunología.
La solicitud de Roche ante la FDA para tratar la nefritis lúpica estuvo respaldada por un ensayo clínico de fase 3 controlado con placebo que evaluó Gazyva además de la terapia estándar: inmunosupresores y antiinflamatorios. Los resultados mostraron que casi el 46,4% de los participantes en el grupo del fármaco del estudio lograron una respuesta renal completa, en comparación con el 33,1% de los que recibieron un placebo y terapias estándar. Los resultados también mostraron mejoras clínicamente significativas en la medición de los niveles de proteínas indicativos de enfermedades autoinmunes y una reducción en el consumo de corticosteroides.
La seguridad de Gazyva fue consistente con el perfil del fármaco en los cánceres de sangre. Las reacciones adversas más comunes notificadas en los ensayos clínicos sobre el cáncer incluyeron reacciones relacionadas con la infusión; niveles anormalmente bajos de neutrófilos, un tipo de glóbulo blanco; e infecciones del tracto respiratorio superior.
“Las personas con nefritis lúpica que logran una respuesta renal completa tienen más probabilidades de conservar la función renal y retrasar o incluso prevenir la progresión a una enfermedad renal terminal”, dijo en una declaración preparada Levi Garraway, director médico y jefe de desarrollo global de productos de Roche. “La aprobación de Gazyva por parte de la FDA representa un paso importante hacia un posible nuevo estándar de atención para la nefritis lúpica que podría permitir a los médicos proporcionar un control más eficaz de la enfermedad a sus pacientes”.
Con la nueva aprobación de Gazyva, Roche puede ofrecer a los pacientes una alternativa biológica al ya establecido producto de GSK, Benlysta, un anticuerpo que inhibe BlyS, una proteína crucial para la supervivencia de las células B. La aprobación de Benlysta por la FDA para tratar el lupus eritematoso sistémico en 2011 lo convirtió en el primer producto biológico para la enfermedad autoinmune. En 2020 la droga amplió su etiqueta a la nefritis lúpica. GSK informó £ 1,5 mil millones (aproximadamente $2 mil millones) en ingresos para Benlysta en 2024, un aumento de más del 10% con respecto a los ingresos del año pasado. En 2021, AstraZeneca recibió la aprobación de la FDA para su fármaco biológico Saphnelo, pero este fármaco de anticuerpos solo está aprobado para el lupus eritematoso sistémico.
Gazyva de Roche (Gazyvaro en Europa) está aprobado en 100 países para diversos tipos de cáncer de sangre. Roche registró unas ventas del producto en 2024 de 910 millones de francos suizos (alrededor de 1.150 millones de dólares), un aumento del 12,2% respecto al año anterior. Gazyva todavía se está probando en Europa para el tratamiento de la nefritis lúpica. La semana pasada un comité de la Agencia Europea de Medicamentos aprobación recomendada del producto en enfermedades autoinmunes. Roche pretende seguir ampliando la marca Gazyva. Actualmente se están realizando ensayos clínicos en lupus eritematoso sistémico, nefropatía membranosa, síndrome nefrótico idiopático y niños y adolescentes con nefritis lúpica.
Foto: peterschreiber.media, Getty Images