Cuando Evommune se hizo pública a fines del año pasado, dijo que los datos de una prueba de concepto de uno de sus candidatos a fármaco para la dermatitis atópica estarían disponibles en la primera mitad de 2026. Los resultados ya están disponibles y la compañía informa sobre el fármaco biológico. Se logró el objetivo principal del experimento.Esto muestra el potencial de un nuevo enfoque y una ventaja de dosificación que lo haría competitivo con el exitoso producto de Sanofi, que actualmente domina el tratamiento de esta afección inflamatoria común de la piel.
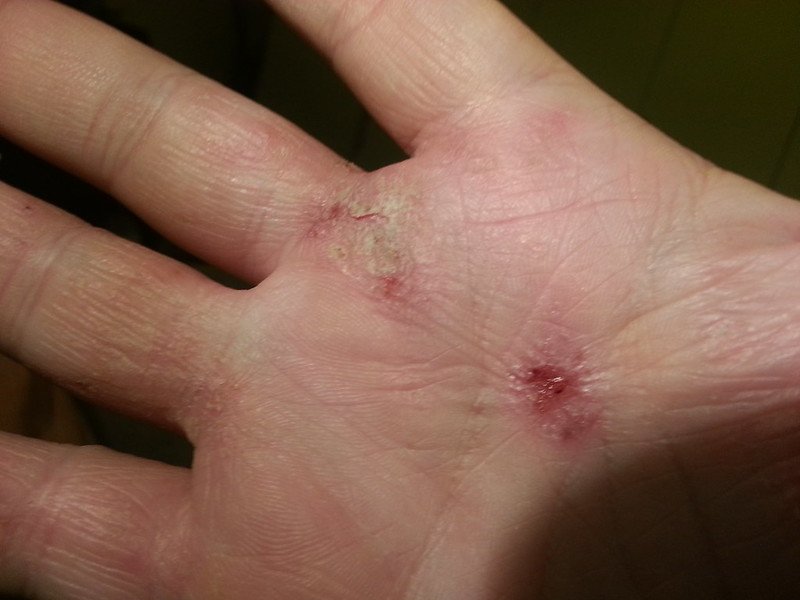
Los datos preliminares sobre el fármaco EVO301 provienen de un ensayo de fase 2a controlado con placebo en el que participaron 70 adultos con dermatitis atópica de moderada a grave, también conocida como eczema. En el estudio de 12 semanas, el fármaco del estudio se calificó utilizando una escala que mide la gravedad de la enfermedad, donde una puntuación más alta indica una enfermedad más grave.
Según los resultados preliminares publicados el martes, EVO301 produjo una reducción estadísticamente significativa en las puntuaciones medidas desde el inicio y en comparación con el placebo en las semanas 4, 8 y 12. El fármaco del estudio, administrado por vía intravenosa al inicio y en la semana 4, fue seguro y bien tolerado; No hubo eventos adversos graves ni interrupciones relacionadas con el tratamiento.
Evommune dijo que los resultados completos se presentarán en una futura conferencia científica. Sin embargo, basándose en los datos preliminares, la compañía con sede en Palo Alto, California, dijo que está avanzando con planes para un estudio de rango de dosis de Fase 2b que pruebe una formulación del medicamento inyectable por vía subcutánea.
Los inversores acogieron con agrado el informe de datos: el precio de las acciones de Evommune abrió a 29,52 dólares el martes, más del 73% más que el precio de cierre del lunes.
EVO301 de Evommune trata la dermatitis atópica apuntando a la IL-18, una proteína de señalización que desempeña un papel en la inflamación. Mientras que Dupixent, un fármaco de anticuerpos de Sanofi y Regeneron Pharmaceuticals, bloquea la señalización de IL-4 e IL-13, Evommune afirma que la neutralización de IL-18 afecta más vías de señalización que impulsan la inflamación en la dermatitis atópica. La empresa biotecnológica está convencida de que este enfoque también podría ser aplicable a otras enfermedades inflamatorias crónicas; Actualmente se está llevando a cabo una prueba de etapa intermedia de EVO301 en la colitis ulcerosa.
EVO301 obtuvo la licencia de la empresa surcoreana AprilBio en 2024. En comparación con los anticuerpos que se dirigen a la IL-18, el diseño de esta proteína de fusión mejora su actividad al tiempo que reduce la probabilidad de desencadenar una respuesta inmune, según Evommune. EVO301 también es de acción prolongada y ofrece la opción de dosificación mensual. En comparación, Dupixent se administra como dosis de mantenimiento cada dos semanas.
El programa Evommune más avanzado es EVO756, que ofrece un enfoque dual para el tratamiento de enfermedades inflamatorias. La pequeña molécula oral se dirige a los mastocitos y las neuronas periféricas bloqueando MRGPRX2, un receptor que se encuentra en ambos objetivos. La empresa cree que este enfoque no sólo combate la inflamación sino que también puede proporcionar un alivio rápido de la picazón. EVO756 ha logrado pruebas separadas de Fase 2b en la enfermedad inflamatoria de la piel, urticaria crónica espontánea y dermatitis atópica de moderada a grave. Se espera la lectura de los datos de ambos estudios a finales de este año.
Evommune salió a bolsa en noviembre pasado, Recaudó 150 millones de dólares en su debut en la Bolsa de Valores de Nueva York bajo el símbolo “EVMN”. La mayoría de los ingresos de la OPI se destinan a planes para hacer avanzar EVO756 a las pruebas de fase 2/3 en urticaria crónica espontánea y dermatitis atópica. La empresa fue fundada por ex ejecutivos de Dermira, una empresa de biotecnología especializada en enfermedades de la piel que fue adquirida por Eli Lilly en 2020. El programa principal de Dermira era un anticuerpo bloqueador de IL-13, que Lilly comercializó como Ebglyss para la dermatitis atópica. Según el Presentación de oferta pública inicial de EvommuneEl compuesto que más tarde se convertiría en EVO756 obtuvo la licencia de Dermira, que está sujeto a pagos por hitos vinculados al desarrollo posterior de la molécula.
En una nota a los inversores, Matt Phipps, analista de William Blair, dijo que los resultados de EVO301 proporcionaron evidencia clara de efectividad en la dermatitis atópica, reforzando un activo cuya valoración el banco creía que apenas se reflejaba en el precio de las acciones de Evommune hasta el martes. Si bien la presentación completa de los datos proporcionará claridad sobre la posición potencial del fármaco en el concurrido mercado de la dermatitis atópica, William Blair ha aumentado la probabilidad de éxito de EVO301 del 29% al 51%. El banco también elevó su estimación de ventas del medicamento para 2035 a mil millones de dólares desde 760 millones de dólares.
“Creemos que esto aún podría resultar conservador, particularmente si se demuestra eficacia en otras enfermedades, como la colitis ulcerosa”, dijo Phipps.
Foto del usuario de Flickr Universidad Estatal de Oregón a través de Creative Commons Licencia